介入式左心室辅助泵广泛应用于心源性休克、体外循环后低心排血量综合征以及高危经皮冠状动脉介入(percutaneous coronary intervention,PCI)等治疗,其应用场景涵盖重症监护室、手术室、急诊科及导管室等各类复杂环境。快速、准确地植入介入式左心室辅助泵并实时监测其位置至关重要。本文报道2例男性高危PCI患者,年龄分别为47岁、45岁,均为冠状动脉三支病变及左心室射血分数降低(<35%)。采用全超声引导技术体系完成国产介入式左心室辅助泵植入,并于介入泵辅助下行PCI治疗,手术过程顺利,2例患者介入泵辅助时间1 h,顺利撤除辅助泵。患者术后无明显介入泵及PCI相关并发症,顺利出院。
介入式左心室辅助泵是一款通过外周血管植入左心室,将左心室血液泵入升主动脉的心脏人工机械辅助产品。与临床常用的体外膜肺氧合及主动脉内球囊反搏相比,介入式左心室辅助泵更符合循环生理,能够有效降低心脏前负荷,明显改善外周灌注,且更加微创[1-3]。目前其已被广泛应用于心源性休克、体外循环后低心排血量综合征以及高危经皮冠状动脉(冠脉)介入(percutaneous coronary intervention,PCI)等治疗,其应用场景涵盖重症监护室、手术室、急诊科、导管室等各类复杂环境[2]。准确植入介入式左心室辅助泵并实时评估监测泵位置,对避免并发症至关重要,超声心动图在其整个应用过程中起到了非常重要的作用[4-6]。目前进口介入式左心室辅助泵价格昂贵且尚未进入我国市场,面对巨大的临床需求[7],我国自主研发的同类产品问世。本文以此为基础,介绍采用单纯超声引导下介入式左心室辅助泵的植入及定位监测经验。
临床资料 患者1,男,47岁,身高166 cm,体重75 kg。9年前急性心肌梗死(心梗)冠脉三支病变,分别于前降支、回旋支及右冠植入3枚支架。1个月前突发胸闷,诊断急性心梗,急性左心衰竭,当地医院治疗后转诊我院,术前评估提示左心室射血分数(ejection fraction,EF)34%,冠脉造影提示前降支支架轻度狭窄,远端斑块狭窄60%,回旋支及右冠支架闭塞。
患者2,男,45岁,身高170 cm,体重64 kg。1+个月前急性心梗,当地医院造影提示冠脉三支病变合并急性左心衰竭,转入我院。术前评估提示患者左冠脉优势型,前降支及回旋支重度狭窄(90%),右冠起源异常合并弥漫性钙化闭塞,EF 34%。
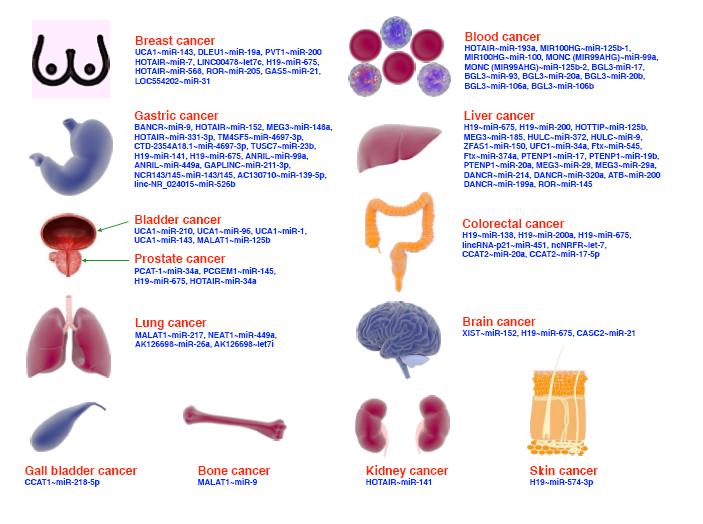
2例患者均为冠脉三支病变,EF<35%且合并左心功能不全表现,经心脏团队评估符合介入式左心室辅助泵辅助下高危PCI介入治疗指征。术前外周血管CT血管造影评价血管入路可,无明显钙化迂曲。此次手术选择国产介入式左心室辅助泵(Renata 5.0,炫脉医疗,上海),其能提供高达5 L/min的全流量左心室辅助,外径21F,采用22F血管鞘输送(图1)。
 图1
国产介入式左心室辅助泵Renata 5.0设计细节
图1
国产介入式左心室辅助泵Renata 5.0设计细节
手术采用局部麻醉+镇静模式,模拟重症监护室及非导管室环境,均采用单纯超声引导植入Renata 5.0介入式左心室辅助泵(使用飞利浦CVX超声系统配合S5-1及L12-3血管超声探头)。首先采用血管超声引导股动脉穿刺,穿刺点为股动脉分叉上方腹腔以下血管段管壁正上方,避免穿刺斑块及钙化(图2a~b)。穿刺成功后植入10F血管鞘,预埋2根Proglide血管缝合器,测算穿刺点距胸骨柄工作距离。采用6F猪尾巴导管及超滑导丝将猪尾导管送入腹主动脉,更换超声引导导丝,在超声引导下将猪尾巴导管送入主动脉弓(图2c),采用胸骨上窝声窗确认。移除超声引导导丝,送入Lunderquist超硬导丝至降主动脉,超声辅助下植入22F Gore输送鞘。再次送入猪尾巴导管,在超滑导丝/超声引导导丝辅助及经胸超声引导下,将猪尾巴导管送入左心室,位于心尖部(图2d~e)。更换0.018支撑导丝(波士顿科学,美国)作为介入泵输送导丝,通过22F输送系统植入介入式左心室辅助泵,采用胸骨旁长轴切面引导,沿导丝经过主动脉送入左心室。患者1主动脉瓣与二尖瓣环平面角度<110°,首次送入介入泵位置出现不良旋转并指向左心室后壁,经过回撤及旋转调整,准确植入左心室(图2f~g)。患者2主动脉瓣与二尖瓣环平面角度可,左心室辅助泵轻松植入左心室,超声引导下显示植入位置过深,回撤调整至主动脉瓣下3.5 cm理想位置(图2h~i)。2例患者PCI手术顺利,介入式左心室辅助泵开机后血压及循环平稳(估测平均辅助流量为3~4 L/min),术中使用超声每半小时确认泵的位置,病变靶血管成功开通。2例患者介入泵辅助时间均为1 h,PCI术后撤出辅助泵,关闭血管通路。患者术后恢复良好,无明显并发症,术后6 h游离血红蛋白<40 mg/L,均顺利出院。
 图2
超声引导介入左心泵植入流程
图2
超声引导介入左心泵植入流程
a~b:超声引导血管穿刺植入22F血管鞘;c:超声引导导丝引导下猪尾巴导管准确进入主动脉弓;d~e:引导导丝及猪尾巴导管进入左心室;f~g:患者1介入泵植入,由于主动脉瓣二尖瓣瓣环角度偏小,介入泵初始位置不佳,经过调整后达到合理位置;h~i:患者2介入泵植入,初始位置较深,超声判定后回撤介入泵达到理想位置
本研究经我院伦理委员会批准(2023-076-01),纳入器械上市前FIM(first-in-man)临床研究,患者均签署知情同意书。
讨论 世界上最具代表性的介入辅助泵(强生医疗,美国)目前具备半流量辅助的Impella CP型号(2~3 L/min)及全流量辅助的5.0型号(5 L/min)。准确植入介入式左心室辅助泵是保证其平稳工作、减少并发症(如溶血、主动脉瓣/二尖瓣损伤、泵失效等)的关键。介入式左心室辅助泵植入理想位置为:(1)泵体深入主动脉瓣下方3.5 cm左右;(2)位于左心室心腔内与心室壁及二尖瓣解剖结构无接触。由于心脏为跳动器官,植入及运行过程需要避免过深(可能导致左心室肌肉损伤、二尖瓣损伤、泵失效)或过浅(主动脉瓣损伤、泵失效),且需要考虑心脏波动对泵位置的影响,目前主要通过介入泵自带的压力监测泵及影像学手段对泵位置及功能进行判定。在诸多临床使用场景中,不同于放射线,床旁超声是最容易获取也是能够提供从血管入路至心室全程引导的影像学手段,配合本团队独创的介入手术超声引导技术体系及器械(包括体外工作距离测量、全程超声图像监测、超声引导导丝等)[8-9],临床医生可在无放射线引导的各类复杂医疗环境下快速准确植入介入式左心室辅助泵。本研究采用的国产Renata 5.0介入式左心室辅助泵对标Impella 5.0,其可提供高达5 L/min的心脏全流量辅助,采用经皮外周血管入路植入的情况下(血管入路条件允许),基本可以满足几乎所有临床场景左心室辅助的治疗需求。研究[10]显示,左心室及主动脉根部解剖差异可导致植入介入式辅助泵位置出现异常,尤其是主动脉瓣及二尖瓣环夹角过小(<126°)或室间隔明显肥厚可导致泵位置不佳,泵体出现旋转并贴靠二尖瓣瓣叶及左心室后壁,此时需要及时调整泵的植入深度并进行适当旋转,避免损伤瓣叶及心室肌肉。对于本研究中患者1,超声及时发现介入泵位置不佳,通过旋转及回撤,准确调整到正确位置。同时如前所述,介入式辅助泵植入的深浅也尤为关键,患者2中,精确的超声图像引导下,术者可对泵的位置进行精确调整,从而确保泵的正常运行。
需要指出的是,本病例虽然实际应用场景为拥有导管室X线的高危PCI患者,由于目前我国自主研发的相关产品极少,无同类进口产品可用,相关技术开展极为有限。研究团队在充分保证患者安全的前提下,进一步证实了单纯超声引导下全临床场景介入式左心室辅助泵植入及定位的可行性,为未来该类技术的普及提供了临床经验。
利益冲突:无。
作者贡献:朱达、王首正、潘湘斌参与论文设计,数据整理与分析;朱达撰写论文初稿;欧阳文斌、王首正、邱洪参与临床治疗全过程;潘湘斌进行论文审阅与修改。
介入式左心室辅助泵是一款通过外周血管植入左心室,将左心室血液泵入升主动脉的心脏人工机械辅助产品。与临床常用的体外膜肺氧合及主动脉内球囊反搏相比,介入式左心室辅助泵更符合循环生理,能够有效降低心脏前负荷,明显改善外周灌注,且更加微创[1-3]。目前其已被广泛应用于心源性休克、体外循环后低心排血量综合征以及高危经皮冠状动脉(冠脉)介入(percutaneous coronary intervention,PCI)等治疗,其应用场景涵盖重症监护室、手术室、急诊科、导管室等各类复杂环境[2]。准确植入介入式左心室辅助泵并实时评估监测泵位置,对避免并发症至关重要,超声心动图在其整个应用过程中起到了非常重要的作用[4-6]。目前进口介入式左心室辅助泵价格昂贵且尚未进入我国市场,面对巨大的临床需求[7],我国自主研发的同类产品问世。本文以此为基础,介绍采用单纯超声引导下介入式左心室辅助泵的植入及定位监测经验。
临床资料 患者1,男,47岁,身高166 cm,体重75 kg。9年前急性心肌梗死(心梗)冠脉三支病变,分别于前降支、回旋支及右冠植入3枚支架。1个月前突发胸闷,诊断急性心梗,急性左心衰竭,当地医院治疗后转诊我院,术前评估提示左心室射血分数(ejection fraction,EF)34%,冠脉造影提示前降支支架轻度狭窄,远端斑块狭窄60%,回旋支及右冠支架闭塞。
患者2,男,45岁,身高170 cm,体重64 kg。1+个月前急性心梗,当地医院造影提示冠脉三支病变合并急性左心衰竭,转入我院。术前评估提示患者左冠脉优势型,前降支及回旋支重度狭窄(90%),右冠起源异常合并弥漫性钙化闭塞,EF 34%。
2例患者均为冠脉三支病变,EF<35%且合并左心功能不全表现,经心脏团队评估符合介入式左心室辅助泵辅助下高危PCI介入治疗指征。术前外周血管CT血管造影评价血管入路可,无明显钙化迂曲。此次手术选择国产介入式左心室辅助泵(Renata 5.0,炫脉医疗,上海),其能提供高达5 L/min的全流量左心室辅助,外径21F,采用22F血管鞘输送(图1)。
 图1
国产介入式左心室辅助泵Renata 5.0设计细节
图1
国产介入式左心室辅助泵Renata 5.0设计细节
手术采用局部麻醉+镇静模式,模拟重症监护室及非导管室环境,均采用单纯超声引导植入Renata 5.0介入式左心室辅助泵(使用飞利浦CVX超声系统配合S5-1及L12-3血管超声探头)。首先采用血管超声引导股动脉穿刺,穿刺点为股动脉分叉上方腹腔以下血管段管壁正上方,避免穿刺斑块及钙化(图2a~b)。穿刺成功后植入10F血管鞘,预埋2根Proglide血管缝合器,测算穿刺点距胸骨柄工作距离。采用6F猪尾巴导管及超滑导丝将猪尾导管送入腹主动脉,更换超声引导导丝,在超声引导下将猪尾巴导管送入主动脉弓(图2c),采用胸骨上窝声窗确认。移除超声引导导丝,送入Lunderquist超硬导丝至降主动脉,超声辅助下植入22F Gore输送鞘。再次送入猪尾巴导管,在超滑导丝/超声引导导丝辅助及经胸超声引导下,将猪尾巴导管送入左心室,位于心尖部(图2d~e)。更换0.018支撑导丝(波士顿科学,美国)作为介入泵输送导丝,通过22F输送系统植入介入式左心室辅助泵,采用胸骨旁长轴切面引导,沿导丝经过主动脉送入左心室。患者1主动脉瓣与二尖瓣环平面角度<110°,首次送入介入泵位置出现不良旋转并指向左心室后壁,经过回撤及旋转调整,准确植入左心室(图2f~g)。患者2主动脉瓣与二尖瓣环平面角度可,左心室辅助泵轻松植入左心室,超声引导下显示植入位置过深,回撤调整至主动脉瓣下3.5 cm理想位置(图2h~i)。2例患者PCI手术顺利,介入式左心室辅助泵开机后血压及循环平稳(估测平均辅助流量为3~4 L/min),术中使用超声每半小时确认泵的位置,病变靶血管成功开通。2例患者介入泵辅助时间均为1 h,PCI术后撤出辅助泵,关闭血管通路。患者术后恢复良好,无明显并发症,术后6 h游离血红蛋白<40 mg/L,均顺利出院。
 图2
超声引导介入左心泵植入流程
图2
超声引导介入左心泵植入流程
a~b:超声引导血管穿刺植入22F血管鞘;c:超声引导导丝引导下猪尾巴导管准确进入主动脉弓;d~e:引导导丝及猪尾巴导管进入左心室;f~g:患者1介入泵植入,由于主动脉瓣二尖瓣瓣环角度偏小,介入泵初始位置不佳,经过调整后达到合理位置;h~i:患者2介入泵植入,初始位置较深,超声判定后回撤介入泵达到理想位置
本研究经我院伦理委员会批准(2023-076-01),纳入器械上市前FIM(first-in-man)临床研究,患者均签署知情同意书。
讨论 世界上最具代表性的介入辅助泵(强生医疗,美国)目前具备半流量辅助的Impella CP型号(2~3 L/min)及全流量辅助的5.0型号(5 L/min)。准确植入介入式左心室辅助泵是保证其平稳工作、减少并发症(如溶血、主动脉瓣/二尖瓣损伤、泵失效等)的关键。介入式左心室辅助泵植入理想位置为:(1)泵体深入主动脉瓣下方3.5 cm左右;(2)位于左心室心腔内与心室壁及二尖瓣解剖结构无接触。由于心脏为跳动器官,植入及运行过程需要避免过深(可能导致左心室肌肉损伤、二尖瓣损伤、泵失效)或过浅(主动脉瓣损伤、泵失效),且需要考虑心脏波动对泵位置的影响,目前主要通过介入泵自带的压力监测泵及影像学手段对泵位置及功能进行判定。在诸多临床使用场景中,不同于放射线,床旁超声是最容易获取也是能够提供从血管入路至心室全程引导的影像学手段,配合本团队独创的介入手术超声引导技术体系及器械(包括体外工作距离测量、全程超声图像监测、超声引导导丝等)[8-9],临床医生可在无放射线引导的各类复杂医疗环境下快速准确植入介入式左心室辅助泵。本研究采用的国产Renata 5.0介入式左心室辅助泵对标Impella 5.0,其可提供高达5 L/min的心脏全流量辅助,采用经皮外周血管入路植入的情况下(血管入路条件允许),基本可以满足几乎所有临床场景左心室辅助的治疗需求。研究[10]显示,左心室及主动脉根部解剖差异可导致植入介入式辅助泵位置出现异常,尤其是主动脉瓣及二尖瓣环夹角过小(<126°)或室间隔明显肥厚可导致泵位置不佳,泵体出现旋转并贴靠二尖瓣瓣叶及左心室后壁,此时需要及时调整泵的植入深度并进行适当旋转,避免损伤瓣叶及心室肌肉。对于本研究中患者1,超声及时发现介入泵位置不佳,通过旋转及回撤,准确调整到正确位置。同时如前所述,介入式辅助泵植入的深浅也尤为关键,患者2中,精确的超声图像引导下,术者可对泵的位置进行精确调整,从而确保泵的正常运行。
需要指出的是,本病例虽然实际应用场景为拥有导管室X线的高危PCI患者,由于目前我国自主研发的相关产品极少,无同类进口产品可用,相关技术开展极为有限。研究团队在充分保证患者安全的前提下,进一步证实了单纯超声引导下全临床场景介入式左心室辅助泵植入及定位的可行性,为未来该类技术的普及提供了临床经验。
利益冲突:无。
作者贡献:朱达、王首正、潘湘斌参与论文设计,数据整理与分析;朱达撰写论文初稿;欧阳文斌、王首正、邱洪参与临床治疗全过程;潘湘斌进行论文审阅与修改。